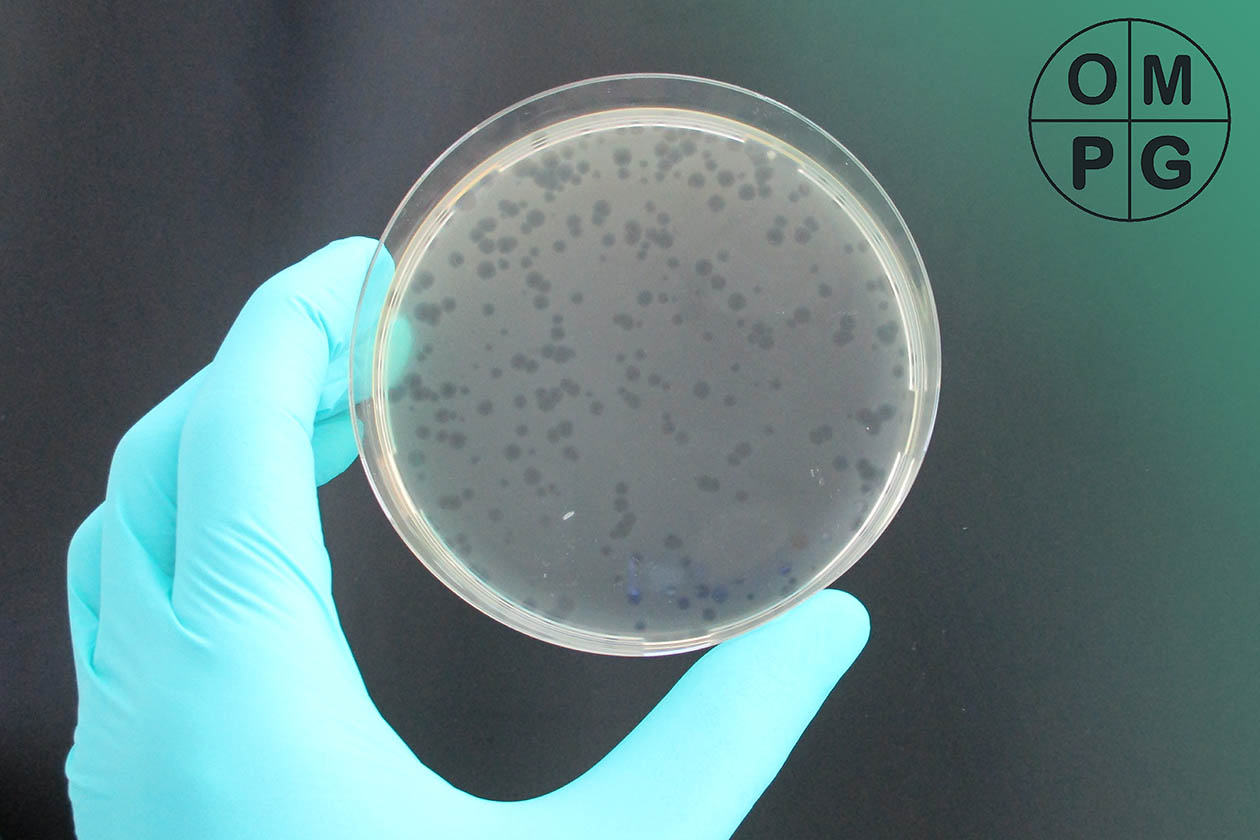
Plaquetitertest des Bakteriophagen phi6. (Bildrechte: OMPG)
Für die Prüfung antiviraler Materialien existieren internationale Standards, darunter die ISO 18184 (Bestimmung der antiviralen Aktivität von Textilerzeugnissen) und die ISO 21702 (Messung der antiviralen Aktivität an Kunststoffen und anderen nicht-porösen Oberflächen). Beide Normen legen als Testorganismen das Influenza-A-Virus (Grippevirus) und das Feline Calicivirus (FCV, Katzenschnupfen) zu Grunde.
„Da Anzucht und Kultivierung von Viren, im Speziellen von humanpathogenen Viren, in Zellkulturen relativ aufwändig sind, hat die OMPG die Prüfungen auf antivirale Wirksamkeit durch die Verwendung von Bakteriophagen deutlich vereinfacht“, sagt Dr. Thomas Dauben, Laborleiter Biologie. „Bakteriophagen infizieren spezifisch Bakterien und sind daher nicht nur einfacher und schneller zu kultivieren als die normgeforderten Viren, sondern stellen zudem auch kein Gesundheitsrisiko für den Menschen dar.“
Der von der OMPG verwendete Bakteriophagen phi6 gehört zur Gattung der Cystoviren und damit zur einzigen Bakteriophagen-Familie mit einer vollständigen Virushülle. Aufgrund dieser morphologischen Eigenschaft verfügt der Bakteriophage auch über einen Vermehrungszyklus, der mit jenem von anderen behüllten humanpathogenen Viren, wie Influenza A oder SARS-CoV-2, vergleichbar ist. „Aus diesem Grund eignet er sich hervorragend als Surrogatvirus – also als vergleichbarer Alternativvirus – für derartige humanpathogene Viren“, so Dr. Dauben. Folglich können mit der von der OMPG modifizierten Prüfmethode nun die antiviralen Prüfungen von Textilien und Kunststoffen einfacher und effizienter durchgeführt werden.
Die Weiterentwicklung von Prüfmethoden durch die OMPG läuft auch mit der Materialforschung am Thüringischen Institut für Textil- und Kunststoff-Forschung (TITK) Hand in Hand. Dort ist die antimikrobielle Ausrüstung von Kunststoffen seit langem ein wichtiger Arbeitsgegenstand. Sowohl eigens entwickelte antibakterielle Silber- und Zink-basierte Additive als auch antivirale Beschichtungen wurden bereits im Rahmen von Forschungsprojekten untersucht.
Hintergrund: Ablauf einer Prüfung auf antibakterielle und antivirale Wirksamkeit
Die Prüfverfahren sind an die jeweiligen antibakteriellen Prüfnormen für Textilien (DIN EN ISO 20743) und Kunststoffe (ISO 22196) angelehnt: Hierbei werden jeweils zwei Bakterienarten, ein gram-positives und ein gram-negatives Bakterium, für die Testung verwendet. Diese werden in einer definierten Zellzahl auf die Proben aufgebracht und nach einer Kontaktzeit von 24 Stunden wieder abgelöst. Anschließend wird die Lebendzellzahl im Vergleich zu einem Kontrollmaterial bestimmt. Die Keimzahlreduktion entspricht der antibakteriellen Wirksamkeit. Für diese Prüfungen ist die OMPG bereits von der Deutschen Akkreditierungsstelle (DAkkS) und der Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten (ZLG) akkreditiert.
Analog hierzu werden antivirale Prüfungen durchgeführt: Eine vorgegebene Anzahl an Viren wird auf die Proben aufgetragen und nach zwei Stunden (Textilien) bzw. 24 Stunden (Kunststoffe) wieder abgelöst. Die Anzahl der Viren wird dann mittels eines Plaquetitertests bestimmt, indem die Viren in einer dekadischen Verdünnungsreihe auf einen Zellrasen aufgebracht und die entstehenden zellfreien Zonen, sogenannte „Plaques“, gezählt werden. Daraus kann der Virustiter auf den Proben berechnet und im Vergleich zu einem nicht antiviral-ausgerüsteten Kontrollmaterial die Virusreduktion ermittelt werden. Diese Reduktion entspricht der antiviralen Wirksamkeit.